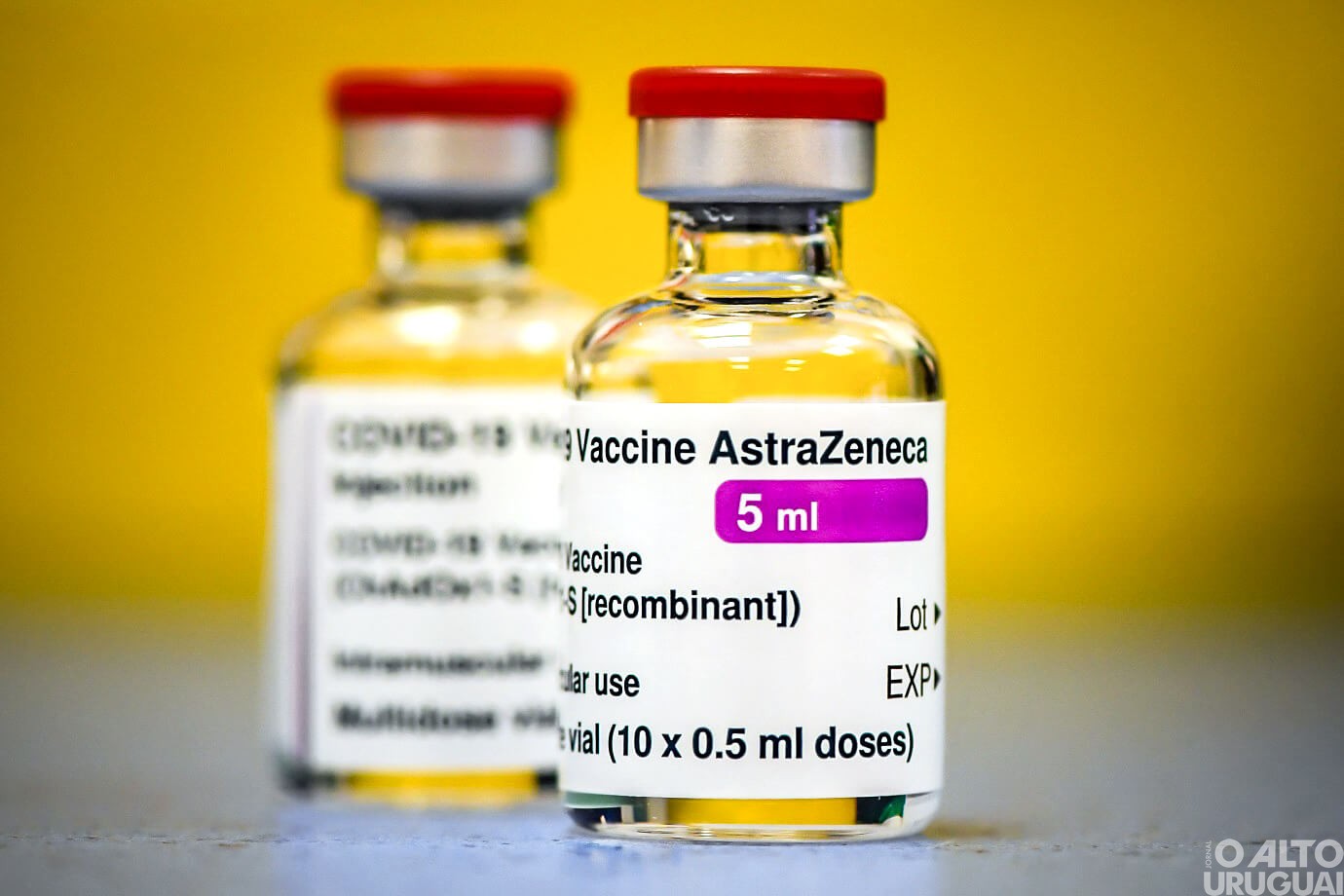
A Agência Nacional de Vigilância Sanitária (Anvisa) concluiu o processo para que o Brasil comece a distribuição da vacina AstraZeneca produzida 100% em território nacional. De acordo com o anúncio, divulgado nesta sexta-feira, 7, a novidade é a aprovação do Insumo Farmacêutico Ativo (IFA), fabricado no país pela própria Fundação Oswaldo Cruz (Fiocruz).
Em nota divulgada, a entidade cita que “a Anvisa avaliou os estudos de comparabilidade. Estes estudos demonstram que, ao ser fabricada no país, o insumo mantém o mesmo desempenho que a vacina importada”, declarou.
Em maio de 2021, a Fiocruz já havia obtido a Certificação de Boas Práticas de Fabricação do novo insumo, etapa que atesta que o local de produção cumpre com os requisitos necessários para garantir uma vacina de qualidade. “Desde então, a Fiocruz vinha realizando a produção de lotes testes para obter a autorização de uso do IFA nacional na vacina Covid-19”, informou representantes da Anvisa.
Com a conclusão do processo, toda a produção da AstraZeneca será feita no Brasil, não dependendo mais da importação do IFA internacional. A transferência de tecnologia começou a ser negociada em 2020 e foi formalizada em junho de 2021.
A expectativa inicial do Ministério da Saúde era de começar a entrega das primeiras doses 100% nacionais em outubro do ano passado, com capacidade de produção de 15 milhões de doses da vacina por mês. No entanto, a Fiocruz só poderia disponibilizar as doses ao Programa Nacional de Imunizações (PNI) após aprovação da Anvisa.
O Brasil possui cinco lotes de IFA nacional produzidos e outros três estão em fase de preparo na Fiocruz. Os lotes ainda passarão pelo processamento final de formulação, envase, revisão, rotulagem e embalagem antes da entrega ao Ministério da Saúde.